Y ahora que aprovecho a cerrar este blog, como último trabajo que hago en este curso y en este colegio, quiero agradecer a todos y a cada uno de los profesores que he tenido, todo lo que me han enseñado. Agradecerles también su paciencia y el apoyo a lo largo de 13 años. Les deseo mucha suerte a todos, y que sepan, que esta alumna siempre se acordará de ellos.
Un beso muy grande, Carmen :)
4ºESO: Física y Química
jueves, 13 de junio de 2013
Excepciones de los hidruros
AMONIACO >>> NH3
FOSFINA >>> PH3
ARSINA >>> ArH3
ESTIBINA >>> SbH3
METANO >>> CH4
SILANO >>> SH4
BORANO >>> BH4

FOSFINA >>> PH3
ARSINA >>> ArH3
ESTIBINA >>> SbH3
METANO >>> CH4
SILANO >>> SH4
BORANO >>> BH4


martes, 11 de junio de 2013
Compuestos más importantes
ÓXIDOS: Combinación de un elemento con el oxígeno.
Fe2O3 >>> Óxido férrico/Trióxido de dihierro
C2O >>> Anhídrido carbónico
CO2 >>> Dióxido de carbono
PERÓXIDOS: Contienen el grupo O2. No se pueden simplificar.
H2O2 >>> Peróxido de dihidrógeno
BeO2 >>> Peróxido de berilio
HIDRUROS: Combinación de un elemento con un hidrógeno.
KH >>> Hidruro potásico/Hidruro de potasio
FeH3 >>> Hidruro férrico/Hidruro de hierro (III)
HCl >>> Ácido clorhídrico/Cloruro de hidrógeno
HIDRÓXIDOS: Combinación de un metal + un elemento del grupo OH.
NaOH >>> Hidróxido de sodio/Hidróxido de sodio
Co(OH)2 >>> Hidróxido cobaltoso/Hidróxido de cobalto (II)
OXOÁCIDOS: Anhídrido + agua (H2O)
H2CO3 >>> Ácido carbónico/Trioxocarbonato(IV) de hidrógeno/Ácido trioxocarbónico (IV)
HNO2 >>> Ácido nitroso/Dioxo nitroso (II) de hidrógeno/Ácido dioxo nítrico (V)
SALES: Reacción entre un ácido + hidróxido
NaCl + H2O >>> Cloruro de sodio
RbClO2 >>> Dioxo clorato (V) de rubidio (I)
MgSO4 >>> Tetraoxo sulfato (VI) de magnesio (II)
Fe2O3 >>> Óxido férrico/Trióxido de dihierro
C2O >>> Anhídrido carbónico
CO2 >>> Dióxido de carbono
PERÓXIDOS: Contienen el grupo O2. No se pueden simplificar.
H2O2 >>> Peróxido de dihidrógeno
BeO2 >>> Peróxido de berilio
HIDRUROS: Combinación de un elemento con un hidrógeno.
KH >>> Hidruro potásico/Hidruro de potasio
FeH3 >>> Hidruro férrico/Hidruro de hierro (III)
HCl >>> Ácido clorhídrico/Cloruro de hidrógeno
HIDRÓXIDOS: Combinación de un metal + un elemento del grupo OH.
NaOH >>> Hidróxido de sodio/Hidróxido de sodio
Co(OH)2 >>> Hidróxido cobaltoso/Hidróxido de cobalto (II)
OXOÁCIDOS: Anhídrido + agua (H2O)
H2CO3 >>> Ácido carbónico/Trioxocarbonato(IV) de hidrógeno/Ácido trioxocarbónico (IV)
HNO2 >>> Ácido nitroso/Dioxo nitroso (II) de hidrógeno/Ácido dioxo nítrico (V)
SALES: Reacción entre un ácido + hidróxido
NaCl + H2O >>> Cloruro de sodio
RbClO2 >>> Dioxo clorato (V) de rubidio (I)
MgSO4 >>> Tetraoxo sulfato (VI) de magnesio (II)
domingo, 9 de junio de 2013
Formulación inorgánica
REGLAS GENERALES DE FORMULACIÓN TRADICIONAL:
-1. Si un elemento tiene 1 valencia: se le nombra con el nombre del elemento o el nombre acabado en -ico.
-2. Si un elemento tiene 2 valencias: Mínimo acabado en -oso, mayor acabado en -ico.
-3. Si un elemento tiene 3 valencias: El mínimo con prefijo hipo- y sufijo -oso. Medio acabado en -oso. Mayor acabado en -ico.
-4. Si un elemento tiene 4 valencias: El mínimo (hipo-nombre-oso). El medio inferior acabado en -oso. El medio superior acabado en -ico. Y el mayor, (per-nombre-ico).
REGLAS GENERALES DE FORMULACIÓN SISTEMÁTICA:
-1. Se nombran los elementos con el prefijo correspondiente al número que halla en la fórmula.
-2. Los prefijos más importantes son: Mono, di, tri, tetra, penta, hexa, y hepta.
REGLAS GENERALES DE LA FORMULACIÓN DE STOCK:
-1. Se nombre el elemento y a continuación se pone la valencia con la que actúa el elemento en la fórmula en números romanos y entre paréntesis.
-2. Cálculo de las valencias en las fórmulas:
A- Todas las valencias son neutras.
B- En oxígeno siempre se forma con carga -2.
C- El hidrógeno en fórmula, actúa con 1.
-1. Si un elemento tiene 1 valencia: se le nombra con el nombre del elemento o el nombre acabado en -ico.
-2. Si un elemento tiene 2 valencias: Mínimo acabado en -oso, mayor acabado en -ico.
-3. Si un elemento tiene 3 valencias: El mínimo con prefijo hipo- y sufijo -oso. Medio acabado en -oso. Mayor acabado en -ico.
-4. Si un elemento tiene 4 valencias: El mínimo (hipo-nombre-oso). El medio inferior acabado en -oso. El medio superior acabado en -ico. Y el mayor, (per-nombre-ico).
REGLAS GENERALES DE FORMULACIÓN SISTEMÁTICA:
-1. Se nombran los elementos con el prefijo correspondiente al número que halla en la fórmula.
-2. Los prefijos más importantes son: Mono, di, tri, tetra, penta, hexa, y hepta.
REGLAS GENERALES DE LA FORMULACIÓN DE STOCK:
-1. Se nombre el elemento y a continuación se pone la valencia con la que actúa el elemento en la fórmula en números romanos y entre paréntesis.
-2. Cálculo de las valencias en las fórmulas:
A- Todas las valencias son neutras.
B- En oxígeno siempre se forma con carga -2.
C- El hidrógeno en fórmula, actúa con 1.
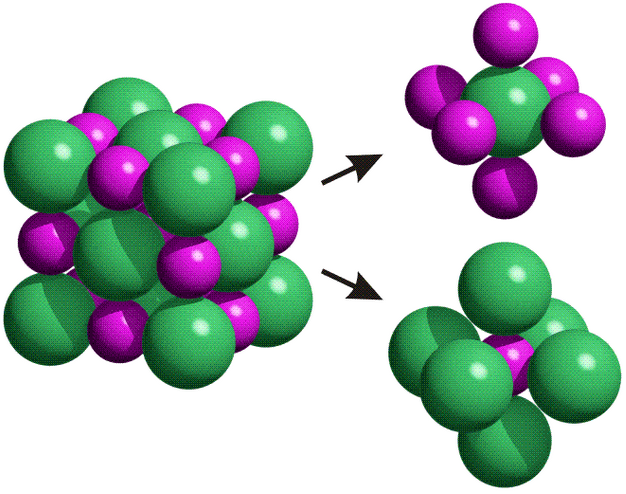
Enlace iónico!
El enlace iónico se basa en la trasferencia de electrones y consiste en la atracción electrostática entre iones con cargas opuestas.
Este tipo de enlaces se establece entre elementos metálicos y no metálicos, y tiene unas propiedades muy diferentes a las de el enlace covalente:
-Son sólidos cristalinos a temperatura ambiente.
-Los puntos de fusión y ebullición son muy elevados.
-Presentan resistencia a ser rayados.
-Son frágiles.
-Son buenos conductores de la electricidad cuando están fundidos.
-Son malos conductores de la electricidad en estado sólido.
-Son muy solubles en agua.
Este tipo de enlaces se establece entre elementos metálicos y no metálicos, y tiene unas propiedades muy diferentes a las de el enlace covalente:
-Son sólidos cristalinos a temperatura ambiente.
-Los puntos de fusión y ebullición son muy elevados.
-Presentan resistencia a ser rayados.
-Son frágiles.
-Son buenos conductores de la electricidad cuando están fundidos.
-Son malos conductores de la electricidad en estado sólido.
-Son muy solubles en agua.
domingo, 19 de mayo de 2013
Enlace covalente.... y Lewis
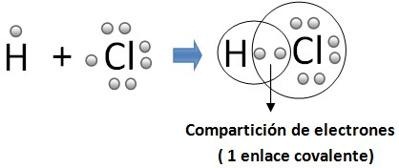
Los átomos que consiguen su estabilidad compartiendo electrones con otros átomos están unidos por un enlace covalente.
Un enlace covalente puede representarse mediante diagramas de puntos conocidos como estructuras de Lewis. El diagrama de Lewis es una forma de representar los electrones de su capa externa. Consiste en escribir el símbolo del elementos e indicar mediante puntos o aspas los electrones de dicha capa.
Su uso es solo ilustrativo. No existe diferencia entre los electrones de los diferentes átomos, todos son equivalentes. Y cada par de electrones que constituye un enlace se representa con una línea. Pongamos algunos ejemplos:


Una sustancia covalente muy importante, es el agua, y además, muy especial, porque a pesar de tener moléculas covalentes parecidas a las de otros compuestos, sus propiedades muy diferentes.
Las moléculas de agua en estado sólido, están unidas entre sí formando agrupaciones, y los "huecos" son ocupados por moléculas sueltas.
Y en estado líquido, están fuertemente unidas entre sí y adoptan las formas hexagonales de los cristales de hierro.
miércoles, 15 de mayo de 2013
Elementos básicos para la vida
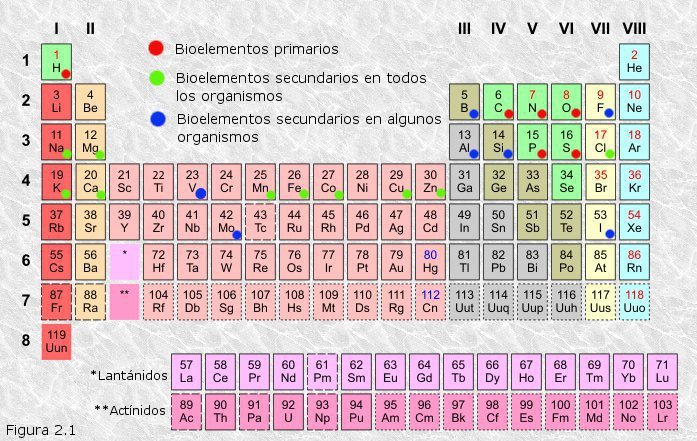
Los elementos químicos que forman parte de la composición de la materia viva se denominan bioelementos. La proporción en que se presentan no es la misma para todos los seres vivos, y por eso se puede clasificar según su abundancia, en tres grupos:
-Bioelementos primarios: Oxígeno, Carbono, Nitrógeno, Hidrógeno, Fósforo y Azufre. Aportan el 96% del total.
-Bioelementos secundarios: Sodio, Potasio, Calcio, Magnesio y Cloro. Son también imprescindibles aunque se encuentren en menor cantidad.
-Oligoelementos: se encuentran en los seres vivos en una proporción menor al 0,1%. Los oligoelementos indispensables, Manganesio, Hierro, Cobalto, Cobre y Zinc, son los que se encuentran en todos los seres vivos.
-Bioelementos primarios: Oxígeno, Carbono, Nitrógeno, Hidrógeno, Fósforo y Azufre. Aportan el 96% del total.
-Bioelementos secundarios: Sodio, Potasio, Calcio, Magnesio y Cloro. Son también imprescindibles aunque se encuentren en menor cantidad.
-Oligoelementos: se encuentran en los seres vivos en una proporción menor al 0,1%. Los oligoelementos indispensables, Manganesio, Hierro, Cobalto, Cobre y Zinc, son los que se encuentran en todos los seres vivos.

Suscribirse a:
Entradas (Atom)