Y ahora que aprovecho a cerrar este blog, como último trabajo que hago en este curso y en este colegio, quiero agradecer a todos y a cada uno de los profesores que he tenido, todo lo que me han enseñado. Agradecerles también su paciencia y el apoyo a lo largo de 13 años. Les deseo mucha suerte a todos, y que sepan, que esta alumna siempre se acordará de ellos.
Un beso muy grande, Carmen :)
jueves, 13 de junio de 2013
Excepciones de los hidruros
AMONIACO >>> NH3
FOSFINA >>> PH3
ARSINA >>> ArH3
ESTIBINA >>> SbH3
METANO >>> CH4
SILANO >>> SH4
BORANO >>> BH4

FOSFINA >>> PH3
ARSINA >>> ArH3
ESTIBINA >>> SbH3
METANO >>> CH4
SILANO >>> SH4
BORANO >>> BH4


martes, 11 de junio de 2013
Compuestos más importantes
ÓXIDOS: Combinación de un elemento con el oxígeno.
Fe2O3 >>> Óxido férrico/Trióxido de dihierro
C2O >>> Anhídrido carbónico
CO2 >>> Dióxido de carbono
PERÓXIDOS: Contienen el grupo O2. No se pueden simplificar.
H2O2 >>> Peróxido de dihidrógeno
BeO2 >>> Peróxido de berilio
HIDRUROS: Combinación de un elemento con un hidrógeno.
KH >>> Hidruro potásico/Hidruro de potasio
FeH3 >>> Hidruro férrico/Hidruro de hierro (III)
HCl >>> Ácido clorhídrico/Cloruro de hidrógeno
HIDRÓXIDOS: Combinación de un metal + un elemento del grupo OH.
NaOH >>> Hidróxido de sodio/Hidróxido de sodio
Co(OH)2 >>> Hidróxido cobaltoso/Hidróxido de cobalto (II)
OXOÁCIDOS: Anhídrido + agua (H2O)
H2CO3 >>> Ácido carbónico/Trioxocarbonato(IV) de hidrógeno/Ácido trioxocarbónico (IV)
HNO2 >>> Ácido nitroso/Dioxo nitroso (II) de hidrógeno/Ácido dioxo nítrico (V)
SALES: Reacción entre un ácido + hidróxido
NaCl + H2O >>> Cloruro de sodio
RbClO2 >>> Dioxo clorato (V) de rubidio (I)
MgSO4 >>> Tetraoxo sulfato (VI) de magnesio (II)
Fe2O3 >>> Óxido férrico/Trióxido de dihierro
C2O >>> Anhídrido carbónico
CO2 >>> Dióxido de carbono
PERÓXIDOS: Contienen el grupo O2. No se pueden simplificar.
H2O2 >>> Peróxido de dihidrógeno
BeO2 >>> Peróxido de berilio
HIDRUROS: Combinación de un elemento con un hidrógeno.
KH >>> Hidruro potásico/Hidruro de potasio
FeH3 >>> Hidruro férrico/Hidruro de hierro (III)
HCl >>> Ácido clorhídrico/Cloruro de hidrógeno
HIDRÓXIDOS: Combinación de un metal + un elemento del grupo OH.
NaOH >>> Hidróxido de sodio/Hidróxido de sodio
Co(OH)2 >>> Hidróxido cobaltoso/Hidróxido de cobalto (II)
OXOÁCIDOS: Anhídrido + agua (H2O)
H2CO3 >>> Ácido carbónico/Trioxocarbonato(IV) de hidrógeno/Ácido trioxocarbónico (IV)
HNO2 >>> Ácido nitroso/Dioxo nitroso (II) de hidrógeno/Ácido dioxo nítrico (V)
SALES: Reacción entre un ácido + hidróxido
NaCl + H2O >>> Cloruro de sodio
RbClO2 >>> Dioxo clorato (V) de rubidio (I)
MgSO4 >>> Tetraoxo sulfato (VI) de magnesio (II)
domingo, 9 de junio de 2013
Formulación inorgánica
REGLAS GENERALES DE FORMULACIÓN TRADICIONAL:
-1. Si un elemento tiene 1 valencia: se le nombra con el nombre del elemento o el nombre acabado en -ico.
-2. Si un elemento tiene 2 valencias: Mínimo acabado en -oso, mayor acabado en -ico.
-3. Si un elemento tiene 3 valencias: El mínimo con prefijo hipo- y sufijo -oso. Medio acabado en -oso. Mayor acabado en -ico.
-4. Si un elemento tiene 4 valencias: El mínimo (hipo-nombre-oso). El medio inferior acabado en -oso. El medio superior acabado en -ico. Y el mayor, (per-nombre-ico).
REGLAS GENERALES DE FORMULACIÓN SISTEMÁTICA:
-1. Se nombran los elementos con el prefijo correspondiente al número que halla en la fórmula.
-2. Los prefijos más importantes son: Mono, di, tri, tetra, penta, hexa, y hepta.
REGLAS GENERALES DE LA FORMULACIÓN DE STOCK:
-1. Se nombre el elemento y a continuación se pone la valencia con la que actúa el elemento en la fórmula en números romanos y entre paréntesis.
-2. Cálculo de las valencias en las fórmulas:
A- Todas las valencias son neutras.
B- En oxígeno siempre se forma con carga -2.
C- El hidrógeno en fórmula, actúa con 1.
-1. Si un elemento tiene 1 valencia: se le nombra con el nombre del elemento o el nombre acabado en -ico.
-2. Si un elemento tiene 2 valencias: Mínimo acabado en -oso, mayor acabado en -ico.
-3. Si un elemento tiene 3 valencias: El mínimo con prefijo hipo- y sufijo -oso. Medio acabado en -oso. Mayor acabado en -ico.
-4. Si un elemento tiene 4 valencias: El mínimo (hipo-nombre-oso). El medio inferior acabado en -oso. El medio superior acabado en -ico. Y el mayor, (per-nombre-ico).
REGLAS GENERALES DE FORMULACIÓN SISTEMÁTICA:
-1. Se nombran los elementos con el prefijo correspondiente al número que halla en la fórmula.
-2. Los prefijos más importantes son: Mono, di, tri, tetra, penta, hexa, y hepta.
REGLAS GENERALES DE LA FORMULACIÓN DE STOCK:
-1. Se nombre el elemento y a continuación se pone la valencia con la que actúa el elemento en la fórmula en números romanos y entre paréntesis.
-2. Cálculo de las valencias en las fórmulas:
A- Todas las valencias son neutras.
B- En oxígeno siempre se forma con carga -2.
C- El hidrógeno en fórmula, actúa con 1.
Enlace iónico!
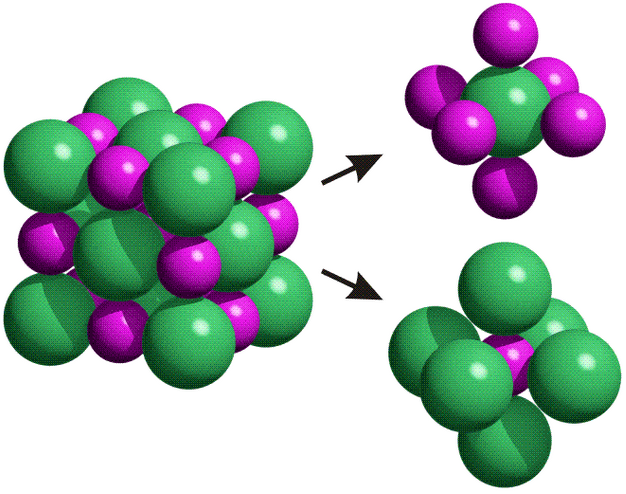
El enlace iónico se basa en la trasferencia de electrones y consiste en la atracción electrostática entre iones con cargas opuestas.
Este tipo de enlaces se establece entre elementos metálicos y no metálicos, y tiene unas propiedades muy diferentes a las de el enlace covalente:
-Son sólidos cristalinos a temperatura ambiente.
-Los puntos de fusión y ebullición son muy elevados.
-Presentan resistencia a ser rayados.
-Son frágiles.
-Son buenos conductores de la electricidad cuando están fundidos.
-Son malos conductores de la electricidad en estado sólido.
-Son muy solubles en agua.
Este tipo de enlaces se establece entre elementos metálicos y no metálicos, y tiene unas propiedades muy diferentes a las de el enlace covalente:
-Son sólidos cristalinos a temperatura ambiente.
-Los puntos de fusión y ebullición son muy elevados.
-Presentan resistencia a ser rayados.
-Son frágiles.
-Son buenos conductores de la electricidad cuando están fundidos.
-Son malos conductores de la electricidad en estado sólido.
-Son muy solubles en agua.
domingo, 19 de mayo de 2013
Enlace covalente.... y Lewis
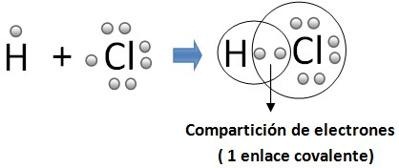
Los átomos que consiguen su estabilidad compartiendo electrones con otros átomos están unidos por un enlace covalente.
Un enlace covalente puede representarse mediante diagramas de puntos conocidos como estructuras de Lewis. El diagrama de Lewis es una forma de representar los electrones de su capa externa. Consiste en escribir el símbolo del elementos e indicar mediante puntos o aspas los electrones de dicha capa.
Su uso es solo ilustrativo. No existe diferencia entre los electrones de los diferentes átomos, todos son equivalentes. Y cada par de electrones que constituye un enlace se representa con una línea. Pongamos algunos ejemplos:


Una sustancia covalente muy importante, es el agua, y además, muy especial, porque a pesar de tener moléculas covalentes parecidas a las de otros compuestos, sus propiedades muy diferentes.
Las moléculas de agua en estado sólido, están unidas entre sí formando agrupaciones, y los "huecos" son ocupados por moléculas sueltas.
Y en estado líquido, están fuertemente unidas entre sí y adoptan las formas hexagonales de los cristales de hierro.
miércoles, 15 de mayo de 2013
Elementos básicos para la vida
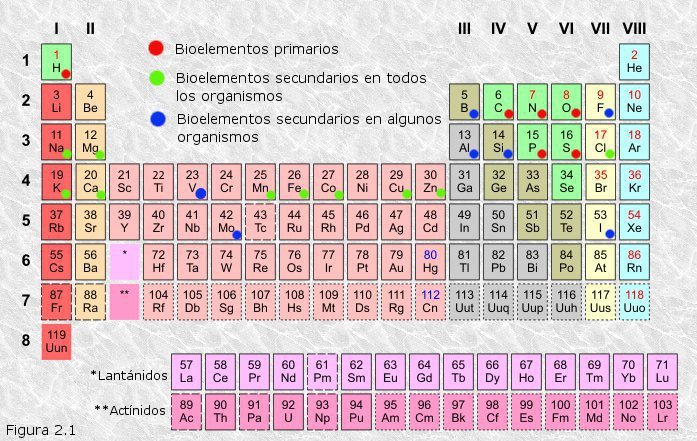
Los elementos químicos que forman parte de la composición de la materia viva se denominan bioelementos. La proporción en que se presentan no es la misma para todos los seres vivos, y por eso se puede clasificar según su abundancia, en tres grupos:
-Bioelementos primarios: Oxígeno, Carbono, Nitrógeno, Hidrógeno, Fósforo y Azufre. Aportan el 96% del total.
-Bioelementos secundarios: Sodio, Potasio, Calcio, Magnesio y Cloro. Son también imprescindibles aunque se encuentren en menor cantidad.
-Oligoelementos: se encuentran en los seres vivos en una proporción menor al 0,1%. Los oligoelementos indispensables, Manganesio, Hierro, Cobalto, Cobre y Zinc, son los que se encuentran en todos los seres vivos.
-Bioelementos primarios: Oxígeno, Carbono, Nitrógeno, Hidrógeno, Fósforo y Azufre. Aportan el 96% del total.
-Bioelementos secundarios: Sodio, Potasio, Calcio, Magnesio y Cloro. Son también imprescindibles aunque se encuentren en menor cantidad.
-Oligoelementos: se encuentran en los seres vivos en una proporción menor al 0,1%. Los oligoelementos indispensables, Manganesio, Hierro, Cobalto, Cobre y Zinc, son los que se encuentran en todos los seres vivos.

martes, 14 de mayo de 2013
Empecemos con química!
Todo, está formado por átomos.
Los átomos estás formados por protones, neutrones y electrones. Según cómo estén dispuestos, junto con sus órbitas y núcleos, se puede diferenciar un elemento de otro.
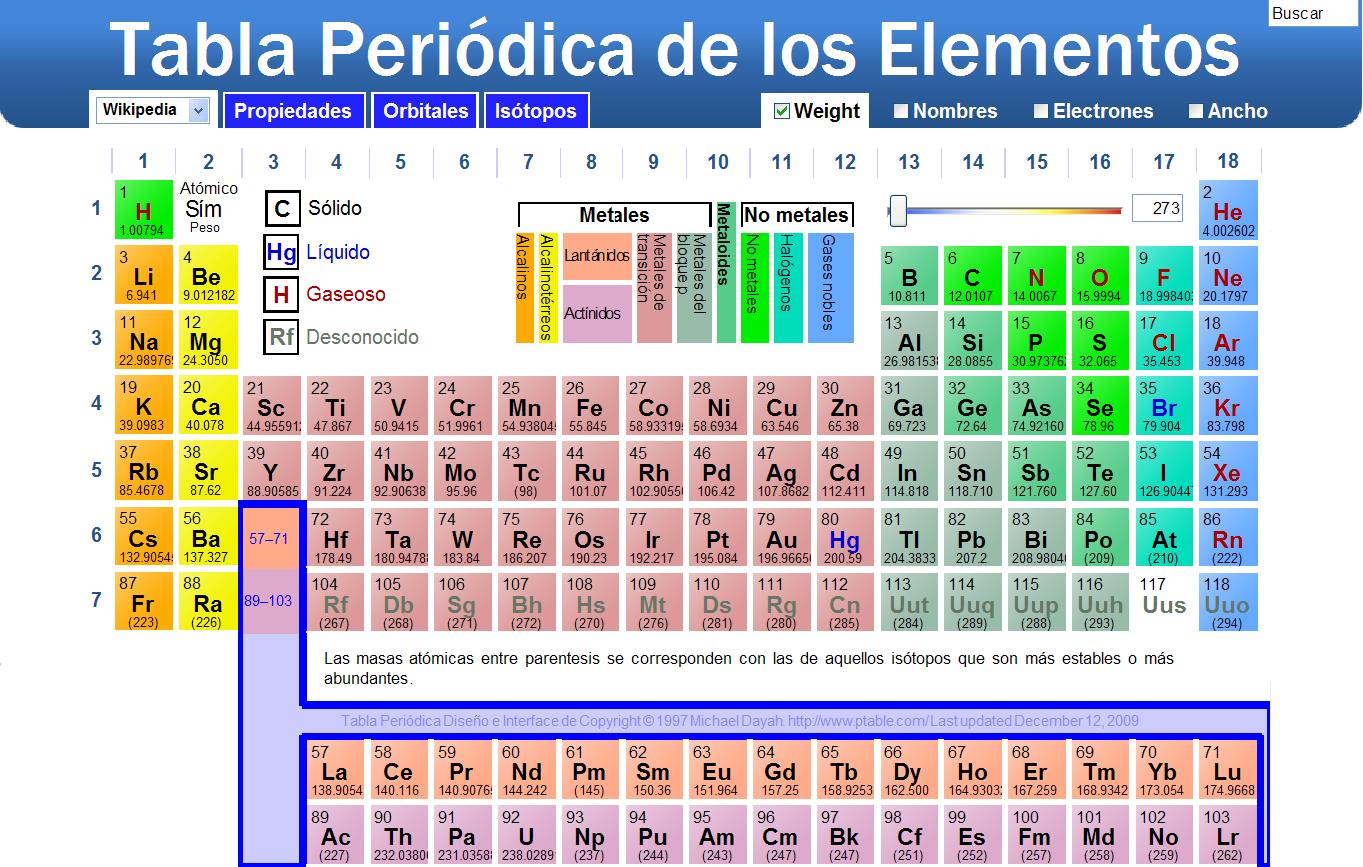
En total hay 117 elementos, ordenados en una tabla dependiendo de sus propiedades y masa atómica y cada uno de ellos tiene un espectro característico de emisión.
En realidad, no se sabe cómo están dispuestas las partículas de los núcleos de los átomos. Pero sí, como giran, cuántas capas tienen y que órbitas siguen. Los primeros que se fijaron en esto, fueron Rutherford, y posteriormente, su ayudante Bohr.
Un átomo puede tener varias capas. Todas ellas van numeradas con una letras y un número. Según la letras que sea, caben un determinado número de electrones:
-Nivel S: 2 electrones
-Nivel F: 6 electrones
-Nivel D: 10 electrones


Los átomos estás formados por protones, neutrones y electrones. Según cómo estén dispuestos, junto con sus órbitas y núcleos, se puede diferenciar un elemento de otro.
En total hay 117 elementos, ordenados en una tabla dependiendo de sus propiedades y masa atómica y cada uno de ellos tiene un espectro característico de emisión.
En realidad, no se sabe cómo están dispuestas las partículas de los núcleos de los átomos. Pero sí, como giran, cuántas capas tienen y que órbitas siguen. Los primeros que se fijaron en esto, fueron Rutherford, y posteriormente, su ayudante Bohr.
Un átomo puede tener varias capas. Todas ellas van numeradas con una letras y un número. Según la letras que sea, caben un determinado número de electrones:
-Nivel S: 2 electrones
-Nivel F: 6 electrones
-Nivel D: 10 electrones

miércoles, 8 de mayo de 2013
Utilidades de las ondas
Todas las ondas que conocemos: sonoras, lumínicas, e incluso radioactivas, tienen alguna utilidad, principalmente las radioactivas:
- Las ondas de radio y televivión, que se utilizan en la comunicación.
-Las microondas, proporcionan vías de comunicación que sustituyen a los cables telefónicos.
-Los rayos ultravioleta, que generan el bronceado.
-Las rayos X, revelan información con una simple fotografía.
-Los rayos gamma, para el tratamiento de cáncer.
-Los infrasonidos, para realizar ecografías.


Fenómenos ondulatorios
Sigamos con las ondas... Hay varios fenómenos que las ondas pueden causar según sean lumínicas, sonoras, o simplemente vibraciones:
Si es luz, las ondas al rebotar, se reflejan con el mismo ángulo absolutamente todas las ondas, ninguna se desvía (claramente si rebotan sobre una superficie lisa).
E incluso pueden refractarse. Cuando un rayo pasa de un medio más denso a otro menos denso, se aleja de la normal y cuando pasa de un medio menos denso a otro más denso, sucede el fenómeno contrario.
Y hay que añadir la difracción, que es el cambio de dirección que experimenta una onda al encontrar un obstáculo inferior a su longitud de onda.


En cambio, las ondas sonoras pueden realizar dos efectos más: el eco, y la reverberación.


Si es luz, las ondas al rebotar, se reflejan con el mismo ángulo absolutamente todas las ondas, ninguna se desvía (claramente si rebotan sobre una superficie lisa).
E incluso pueden refractarse. Cuando un rayo pasa de un medio más denso a otro menos denso, se aleja de la normal y cuando pasa de un medio menos denso a otro más denso, sucede el fenómeno contrario.
Y hay que añadir la difracción, que es el cambio de dirección que experimenta una onda al encontrar un obstáculo inferior a su longitud de onda.


En cambio, las ondas sonoras pueden realizar dos efectos más: el eco, y la reverberación.


Fotoramas!
En la anterior entrada puse unos vídeos sobre un helicóptero, cuyas aspas parecen no se mueven, y unas gotas de agua que incluso parece que se quedan suspendidas en el aire.
Bien, pues esto se produce debido a las cámaras de vídeo. Las cámaras tienen la capacidad de grabar hasta 24 imágenes por segundo. Con este dato, podemos deducir que las aspas del helicóptero daba el mismo número de vueltas por segundo, y daba la impresión de que estaban quietas, y lo mismo podríamos decir con el agua.
Bien, pues esto se produce debido a las cámaras de vídeo. Las cámaras tienen la capacidad de grabar hasta 24 imágenes por segundo. Con este dato, podemos deducir que las aspas del helicóptero daba el mismo número de vueltas por segundo, y daba la impresión de que estaban quietas, y lo mismo podríamos decir con el agua.
jueves, 4 de abril de 2013
WOW!
¿Cómo puede ser esto posible? El próximo día de clase lo descubriremos, mientras echad un vistazo ;)
Energía de la ondas
Hace unos días, comenzamos un tema que trata sobre las ondas y su energía.
Una onda es la posición que adopta en cada instante la perturbación que se ha producido.
Pongámoslo como ejemplo en una cuerda, o con una piedra que cae en el agua:
-En el extremo de la cuerda, el foco, se produce una vibración hacia arriba y abajo que se propaga horizontalmente por toda la cuerda.
-Las moléculas de agua con las que choca la piedra comienzan a vibrar verticalmente y la vibración se transmite horizontalmente a las moléculas próximas a ellas.
Existen varios tipos de ondas: mecánicas, electromagnéticas y transversales.
Y todas ellas se caracterizan por sus magnitudes: velocidad (v), longitud de onda(lambda), período(T), frecuencia(f), amplitud(A) e intensidad(I).
martes, 12 de marzo de 2013
Energía y calor
 Hoy hemos realizado un examen sobre estas dos temáticas que incluye la física, asique voy a hablar un poco de ellas:
Hoy hemos realizado un examen sobre estas dos temáticas que incluye la física, asique voy a hablar un poco de ellas:Se denomina trabajo a la fuerza que se reliza sobre un cuerpo produciendo un movimiento en la misma dirección en la que esta se ejerce. Y se calcula así: W= F*Ax. El trabajo se mide en Julios (J)
Se denomina energía, a la capacidad que tiene un cuerpo de realizar transformaciones o realizar un trabajo.
Hay varios tipos de energía: térmica, mecánica, electromagnética, eléctrica... Pero nos centraremos en la mecánica y en la térmica, el calor.
La energía mecánica es la suma de otras dos energías: la potencial, y la cinética. Depende del movimiento y de la posición del objeto:
Energía cinética= 1/2 * m* v^2
Energía potencial= m*g*h
De estas energías se pueden derivar otras muchas, como la energía potencial elástica: 1/2 *K*Ax^2
o calcular el rendimiento de una máquina: potencia últil/potencia teórica *100
El calor es la transferencia de energía térmica de un cuerpo de mayor temperatura, a otro de menor temperatura. Se denomina equilibrio térmico cuando dos cuerpos en contacto se encuentran a la misma temperatura.
El calor se expresa en Julios (J), y la temperatura en grados centígrados (ºC) o en grados Kelvin (K).
Y se halla de la siguiente manera:
Q= m*Ce (calor específico)* AT (variación de la temperatura)
De esta forma, se pueden resolver problemas utilizando los dos tipos de energía juntas: mecánica y térmica.
domingo, 3 de marzo de 2013
Cálculo de la gravedad: Dinamómetro y péndulo
Hace unos días hemos realizado un experimento en el laboratorio, que consistía en calcular la gravedad de formas diferentes. Con un dinamómetro y un péndulo:
Con el dinamómetro vertimos un líquido: la glicerina. Con la glicerina en la probeta, metimos el cilindro en ella para calcular el
volumen de éste. A continuación medimos
los Newtons que había subido el cilindro en la probeta, como resultado del
empuje de la glicerina. Finalmente con todos los datos necesarios, los
empleamos una fórmula para calcular la gravedad, cuyo resultado es: 9,60 m/s^2
Sin
embargo, con el péndulo, medimos con un cronómetro el tiempo que tardaba un
objeto de plomo colgando de una cuerda de 83,5cm en realizar 5
oscilaciones. Seguidamente calculamos el
tiempo de una oscilación, y con ese dato junto con la medida de la cuerda hasta
el centro de masas del objeto, empleamos otra fórmula diferente para calcular
la gravedad; cuyo resultado fue de: 10m/m^2.
Finalmente el error del experimento fue de 1,5% nada mal para nosotros :)
lunes, 11 de febrero de 2013
Comprimir latas sin usar la fuerza
Hola fisiqueros! Aquí me teneis de nuevo tras estos grandes carnavales, imagino que hayais venido a Santoña, porque como aquí, en ningún sitio :D
Bueno, con lo que iba... Hace unos cuantos días, junto con el experimento de dibujar sobre la leche, hicimos otro diferente en el laborarorio: Comprimir latas sin usar la fuerza. Para ello, necesitamos un mechero bunsen, unas cuantas latas, y un recipiente de agua fría:
1º: Se coje la lata, y se coloca la llama del mechero por el agujero.
2º: Se espera un momento, como se muestra en la fotografía hasta que empiece a quemar
3º: Cuando empiece a quemar, se vierte lo más rapido que se pueda la lata en el agua fría.
4º: Si hemos hecho bien los pasos, las latas quedarán finalmente así:
Bueno, con lo que iba... Hace unos cuantos días, junto con el experimento de dibujar sobre la leche, hicimos otro diferente en el laborarorio: Comprimir latas sin usar la fuerza. Para ello, necesitamos un mechero bunsen, unas cuantas latas, y un recipiente de agua fría:
1º: Se coje la lata, y se coloca la llama del mechero por el agujero.
2º: Se espera un momento, como se muestra en la fotografía hasta que empiece a quemar
3º: Cuando empiece a quemar, se vierte lo más rapido que se pueda la lata en el agua fría.
4º: Si hemos hecho bien los pasos, las latas quedarán finalmente así:
¡Y aquí están los protagonistas!
miércoles, 23 de enero de 2013
¡Obras de arte en física!
Esta misma mañana en la clase de física y química, mis compañeros y yo hemos ido al laboratorio, y hemos realizado dos experimentos: Hacer un dibujo sobre leche, utilizando una gota de jabón, y comprimir latas de refresco sin tocarlas, del cual hablaré más adelante.
-Lo primero, para crear nuestro dibujo, necesitamos un plato de plástico, un poco de leche, unas gotitas de colorante, unos bastoncillos y un poco de jabón.
-Lo primero, para crear nuestro dibujo, necesitamos un plato de plástico, un poco de leche, unas gotitas de colorante, unos bastoncillos y un poco de jabón.
-Ahora, debemos verter unas gotitas de colorante en el centro de la leche.
-Sucesivamente, verteremos en uno de los bastoncillos una gota de jabón, y tocaremos con ello en el colorante, y vualá, mirad lo que pasa:
Obra de arte de Roberto y Germán
Obra de arte de Jaime y Rubén
Obra de arte de los dos Pablos
Obra de arte mía y de Fernanda: ¡Es el universo!
martes, 22 de enero de 2013
Tensión superficial: el experimento del agua y el aceite!
Uno de los apartados del tema "Fuerzas en los fluidos" trata sobre la tensión superficial. Para comprobarlo, el profesor nos retó a realizar un experimento, poniendo en un recipiente agua y una capa de aceite, para más tarde, verter una gota de jabón, y ver lo que pasa...
Aquí están las fotos, con los pasos que he seguido:
-Se vierte agua en un recipiente, en mi caso, un bol, con aceite, y podéis comprobar cómo el aceite tiende a situarse sobre el agua.
-Ahora, ya que tenemos el aceite listo, nos untamos el dedo con una gota de jabón, y la vertéis en el centro de la superficie del aceite. Como resultado, la tensión del aceite se romperá, y se creará un enorme agujero en el centro. En mi caso, esperé un poco más a ver qué sucedía, y finalmente el aceite tendió a juntarse de nuevo, quedando solamente un pequeño agujero.
jueves, 10 de enero de 2013
Contact!
 Contact es una película basada en el libro de Carl Sagan que yo y mis compañeros hemos visto hace unas 2 semanas, que trata sobre cómo sería el primer contacto con vida extraterrestre. Está bastante bien, porque lo representa de una forma muy realista, con las consecuencias y peligros que eso podría conllevar, toda una novedad, para una película de los años 90.
Contact es una película basada en el libro de Carl Sagan que yo y mis compañeros hemos visto hace unas 2 semanas, que trata sobre cómo sería el primer contacto con vida extraterrestre. Está bastante bien, porque lo representa de una forma muy realista, con las consecuencias y peligros que eso podría conllevar, toda una novedad, para una película de los años 90.Por todo esto, hemos tenido que realizar un trabajo sobre Contact y sobre el proyecto SETI, un elemento fundamental a lo largo de toda la película, y gracias a sus científicos, se pudo llevar a cabo el contacto.
Carl Sagan nos ha enseñado con su novela que el misterio más grande en este mundo no se encuentra en lo basto e infinito del universo, simplemente. Y es así como en "Contacto", una astróloga en busca de su propia verdad se da cuenta que realmente no estamos solos, porque de ser asi ¡cuánto espacio desaprovechado!
En mi opinión esta película hace que nos demos cuenta que no estamos preparados para lo desconocido, y que tan solo somos una pequeña fracción de tiempo en la infinidad de eso que conocemos como universo.
martes, 1 de enero de 2013
Viaje a los límites del universo.
¡La primera entrada de 2013! Espero que lo hayáis pasado en grande en Nochevieja, y si os habéis portado bien, esperad a los Reyes Magos este domingo, que alguna cosilla fijo que os traerán. ¡En nada nos vemos fisiqueros! ;)
Bueno, hace unos días vimos un documental titulado: "Viaje a los límites del universo". Ya os podéis imaginar, de que va este documental.
Dirigido por Yavar Abbas, tiene una duración
 de alrededor una hora y media y desvela los misterios del Cosmos. Nos adentra en los secretos del espacio, en un
viaje desde nuestro querido planeta Tierra hasta los confines del universo, hasta el mismísimo origen del "todo", el Big Ban, pasando por numerosas estrellas, nebulosas, galaxias, agujeros de gusano (no se sabe con seguridad si existen), cometas, numerosos planetas...todo ello realizado a partir de la combinación de imágenes reales con otras generadas por
ordenador. Nos muestra una visión sorprendente de los mundos que existen más allá del nuestro, captadas desde las naves espaciales o por los mayores telescopios
del mundo como el Hubble, complementadas con efectos especiales que permiten recrear el primer viaje al espacio infinito. Y sí, también nos da la posibilidad de creer que hay muchas otras civilizaciones al igual que nosotros, sean inteligentes o no, en alguna parte de este inmenso universo, que por diversas razones, todavía no hemos podido presenciar o contactar, y de ahí, la pregunta de si algún día podremos contactar con "algo", o simplemente si existe otra vida aparte de la nuestra, o cómo será nuestro primer contacto... La respuesta a algunas de estas preguntas, las recrea muy bien una película que también vimos acerca de este tema, titulada "Contact", de la cual ya os hablaré más adelante.. Por ahora os dejo el documental por si os interesa verlo :)
de alrededor una hora y media y desvela los misterios del Cosmos. Nos adentra en los secretos del espacio, en un
viaje desde nuestro querido planeta Tierra hasta los confines del universo, hasta el mismísimo origen del "todo", el Big Ban, pasando por numerosas estrellas, nebulosas, galaxias, agujeros de gusano (no se sabe con seguridad si existen), cometas, numerosos planetas...todo ello realizado a partir de la combinación de imágenes reales con otras generadas por
ordenador. Nos muestra una visión sorprendente de los mundos que existen más allá del nuestro, captadas desde las naves espaciales o por los mayores telescopios
del mundo como el Hubble, complementadas con efectos especiales que permiten recrear el primer viaje al espacio infinito. Y sí, también nos da la posibilidad de creer que hay muchas otras civilizaciones al igual que nosotros, sean inteligentes o no, en alguna parte de este inmenso universo, que por diversas razones, todavía no hemos podido presenciar o contactar, y de ahí, la pregunta de si algún día podremos contactar con "algo", o simplemente si existe otra vida aparte de la nuestra, o cómo será nuestro primer contacto... La respuesta a algunas de estas preguntas, las recrea muy bien una película que también vimos acerca de este tema, titulada "Contact", de la cual ya os hablaré más adelante.. Por ahora os dejo el documental por si os interesa verlo :)
Bueno, hace unos días vimos un documental titulado: "Viaje a los límites del universo". Ya os podéis imaginar, de que va este documental.
Dirigido por Yavar Abbas, tiene una duración
 de alrededor una hora y media y desvela los misterios del Cosmos. Nos adentra en los secretos del espacio, en un
viaje desde nuestro querido planeta Tierra hasta los confines del universo, hasta el mismísimo origen del "todo", el Big Ban, pasando por numerosas estrellas, nebulosas, galaxias, agujeros de gusano (no se sabe con seguridad si existen), cometas, numerosos planetas...todo ello realizado a partir de la combinación de imágenes reales con otras generadas por
ordenador. Nos muestra una visión sorprendente de los mundos que existen más allá del nuestro, captadas desde las naves espaciales o por los mayores telescopios
del mundo como el Hubble, complementadas con efectos especiales que permiten recrear el primer viaje al espacio infinito. Y sí, también nos da la posibilidad de creer que hay muchas otras civilizaciones al igual que nosotros, sean inteligentes o no, en alguna parte de este inmenso universo, que por diversas razones, todavía no hemos podido presenciar o contactar, y de ahí, la pregunta de si algún día podremos contactar con "algo", o simplemente si existe otra vida aparte de la nuestra, o cómo será nuestro primer contacto... La respuesta a algunas de estas preguntas, las recrea muy bien una película que también vimos acerca de este tema, titulada "Contact", de la cual ya os hablaré más adelante.. Por ahora os dejo el documental por si os interesa verlo :)
de alrededor una hora y media y desvela los misterios del Cosmos. Nos adentra en los secretos del espacio, en un
viaje desde nuestro querido planeta Tierra hasta los confines del universo, hasta el mismísimo origen del "todo", el Big Ban, pasando por numerosas estrellas, nebulosas, galaxias, agujeros de gusano (no se sabe con seguridad si existen), cometas, numerosos planetas...todo ello realizado a partir de la combinación de imágenes reales con otras generadas por
ordenador. Nos muestra una visión sorprendente de los mundos que existen más allá del nuestro, captadas desde las naves espaciales o por los mayores telescopios
del mundo como el Hubble, complementadas con efectos especiales que permiten recrear el primer viaje al espacio infinito. Y sí, también nos da la posibilidad de creer que hay muchas otras civilizaciones al igual que nosotros, sean inteligentes o no, en alguna parte de este inmenso universo, que por diversas razones, todavía no hemos podido presenciar o contactar, y de ahí, la pregunta de si algún día podremos contactar con "algo", o simplemente si existe otra vida aparte de la nuestra, o cómo será nuestro primer contacto... La respuesta a algunas de estas preguntas, las recrea muy bien una película que también vimos acerca de este tema, titulada "Contact", de la cual ya os hablaré más adelante.. Por ahora os dejo el documental por si os interesa verlo :)
Suscribirse a:
Entradas (Atom)